آبکاری یا همان Plating اصطلاحی است که برای قرار دادن روکش روی فلزات به کار میرود. آبکاری میتواند با فلزات گرانبها مثل طلا و نقره روی فلزاتی نظیر آهن و مس برای زیبایی آنها در وسایلی نظیر قاشق، چنگال و … انجام شود و یا برای افزایش میزان رسانایی و جلوگیری از خوردگی آنها به کار میرود. خوردگی فلز ممکن است به صورت شیمیایی(توسط گازهای خشک و محلولهای روغنی گازوئیل و نفت و یا الکتروشیمیایی انجام پذیرد. طبیعت و میزان خوردگی به ویژگیهای آن فلز، محیط و حرارت وابسته است.
روشهای زیادی برای جلوگیری از خوردگی وجود دارد که یکی از آنها ایجاد روکشی مناسب برای فلزها میباشد و معمولترین روشهای روکش فلزها عبارتنداز: رنگین کردن فلزات، لعابکاری، آبکاری با روکش پلاستیک، حفاظت کاتدیک و آبکاری با فلزات دیگر میباشد.
آبکاری الکتریکی
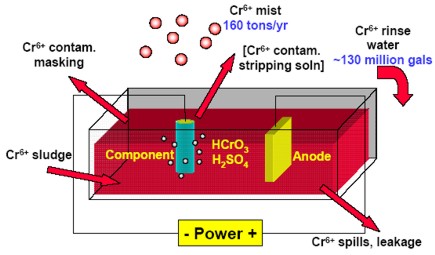
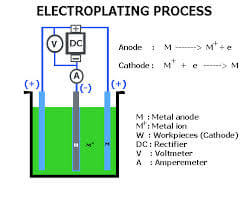
در این روش ترسیب گالوانیک یک فلز بر پایه واکنشهای الکتروشیمیایی صورت میگیرد. هنگام الکترولیز در سطح محدود الکترود/الکترولیت در نتیجه واکنشهای الکتروشیمیایی الکترونها یا دریافت میشوند (احیا) و یا واگذار میشوند (اکسیداسیون برای اینکه واکنشها در جهت واحد مورد نظر ادمه یابند لازم است به طور مداوم از منبع جریان خارجی استفاده شود. در این روش با واکنش الکتروشیمیایی گونه مورد نظر بر روی کاتد قرار میگیرد. واکنشهای مشخص در آند و کاتد همچنین در الکترولیت همیشه به صورت همزمان صورت میگیرند. محلول الکترولیت باید شامل یونهای فلز رسوبکننده باشد و چون یونهای فلزها دارای بار مثبت می باشند به علت جذب بارهای مخالف تمایل به حرکت در جهت الکترود یا قطبی که دارای الکترون اضافی میباشد (قطب منفی یا کاتد) را دارند. قطب مخالف که کمبود الکترون دارد قطب مثبت یا آند نامیده میشود. به طور کلی فرایند معمول پوششدهی را میتوان به صورت زیر در نظر گرفت:
-یک اتم در آند یک یا چند الکترون از دست میدهد و در محلول پوششدهی به صورت یون مثبت در میآید.
-یون مثبت به طرف کاتد یعنی محل تجمع الکترونها جذب شده و در جهت آن حرکت میکند.
- این یون الکترونهای از دست داده را در کاتد به دست آورده و پس از تبدیل به اتم به صورت جزیی از فلز رسوب میکند.
آبکاری بدون استفاده از منبع جریان خارجی
هنگام ترسیب فلز بدون استفاده از منبع جریان خارجی الکترونهای لازم برای احیای یونهای فلزی توسط واکنشهای الکتروشیمیایی تامین میشوند. بر این اساس سه امکان وجود دارد:
ترسیب فلز به روش تبادل بار (تغییر مکان) یا فرایند غوطهوری: اساس کلی این روش بر اصول جدول پتانسیل فلزها پایهریزی شده است. فلزی که باید پوشیده شود باید پتانسیل آن بسیار ضعیفتر (فلز فعال) از پتانسیل فلز پوشنده (فلز نجیب) باشد. و فلزی که باید ترسیب شود باید در محلول به حالت یونی وجود داشته باشد. برای مثال به هنگام غوطهور نمودن یک میله آهنی در یک محلول سولفات مس فلز آهن فعال است و الکترون واگذار میکند و به شکل یون آهن وارد محلول میشود. دو الکترون روی میله آهن باقی میماند. یون مس دو الکترون را دریافت کرده احیا میشود و بین ترتیب مس روی میله آهن میچسبد. و هنگامی که فلز پایه که باید پوشیده شود (مثلا آهن) کاملا″ توسط فلز پوشنده (مثلا مس) پوشیده شود آهن دیگر نمیتواند وارد محلول شود و الکترون تشکیل نمیشود و در نتیجه عمل ترسیب خاتمه مییابد. موارد استعمال این روش در صنعت آبکاری عبارت است از: مساندود نمودن فولاد٬ نقرهکاری مس و برنج، جیوهکاری، حمام زنکات، روشهای مختلف کنترل و یا آزمایش، جمعآوری فلز از حمامهای فلزات قیمتی غیر قابل استفاده (طلا) با استفاده از پودر روی.
ترسیب فلز به روش اتصال این روش عبارت است از ارتباط دادن فلز پایه با یک فلز اتصال. جسم اتصال نقش واگذارکننده الکترون را ایفا میکند. برای مثال هنگامی که یک میله آهنی (فلز پایه) همراه یک میله آلومینیومی، به عنوان جسم اتصال در داخل یک محلول سولفات مس فرو برده میشود، دو فلز آهن و آلومینیوم به جهت فعالتر بودن از مس، به صورت یون فلزی وارد محلول میشوند و روی آنها الکترون باقی میماند و چون فشار انحلال آلومینیوم از آهن بیشتر است از این رو اختلاف پتانسیلی بین دو فلز ایجاد شده و الکترونها در روی یک سیم رابط، از سوی آلومینیوم به طرف آهن جاری میشوند. بنابراین مشاهده میشود که مقدار زیادی از یونهای مس محلول روی آهن ترسیب میشوند. ضخامت قشر ایجاد شده نسبت به روش ساده تبادل بار بسیار ضخیمتر است. از روش اتصال برای پوششکاری فلزات پیچیده استفاده میشود.
روش احیا: ترسیب فلز با استفاده از محلولهای حاوی مواد احیا کننده، روش احیا نامیده میشود. یعنی دراین روش الکترونهای لازم برای احیای یونهای فلزات توسط یک احیا کننده فراهم میشود. پتانسیل احیا کنندهها باید از فلز پوشنده فعالتر باشند، اما بابد خاطر نشان ساخت که اختلاف پتانسیل به دلایل منحصرا″ کاربردی روکشها، نباید بسیار زیاد باشد. برای مثال هیپوفسفیت سدیم یک احیا کننده برای ترسیب نیکل است ولی برای ترسیب مس که نجیبتر است، مناسب نیست. مزیت استفاده از این روش در این است که میتوان لایههایی با ضخامت دلخواه ایجاد نمود. زیرا اگر مقدار ماده احیا کننده در الکترولیت ثابت نگه داشته شود میتوان واکنش ترسیب را کنترل نمود. به ویژه غیر هادیها را نیز بعد از فعال نمودن آنها، میتوان پوششکاری کرد.
موقعیت های استفاده از نانوتکنولوژی صنایع آبکاری
در سالهای اخیر نانوتکنولوژی که همان علم و تکنولوژی کنترل و بکارگیری ماده در مقیاس نانومتر است، تحقیقات گسترده و موقعیتهای تجاری زیادی را در زمینههای مختلف ایجاد نموده است. یک جنبه خاص از نانوتکنولوژی به مواد دارای ساختار نانویی یعنی موادی با بلورهای بسیار ریز که اندازه آنها معمولا کمتر از ۱۰۰ نانومتر است میپردازد، که این مواد برای اولین بار حدود دو دهه قبل به عنوان فصل مشترکی معرفی شدند. این مواد نانوساختاری با سنتز الکتروشیمیایی تولید شدهاند که دارای خواصی از قبیل، استحکام، نرمی و سختی، مقاومت به سایش، ضریب اصطکاک، مقاومت الکتریکی، قابلیت انحلال هیدروژن و نفوذپذیری، مقاومت به خوردگی موضعی و ترک ناشی از خوردگی تنشی و پایداری دمایی را دارا هستند. دریچههای آبکاری الکتریکی برای سنتز این ساختارها با استفاده از تجهیزات و مواد شیمیایی مرسوم برای طیف گسترهای از فلزات خالص و آلیاژها گشوده شده است. یک روش مقرون به صرفه برای تولید محصولاتی با اشکال بسیار متفاوت از پوششهای نازک و ضخیم، فویلها و صفحهها با اشکال غیر ثابت تا اشکال پیچیده شکلیافته با روشهای الکتریکی است. از این رو فرصتهای قابل توجهی برای صنعت آبکاری وجود دارد تا نقش تعیینکنندهای را در گسترش کاربردهای جدید نانوتکنولوژی ایفا نماید که این امر به آسانی با تکیه بر اصول قابل پیشبینی متالوژیکی که در سالیان گذشته مشخص شده قابل تحقق است.
نتیجه گیری:
به طور خلاصه، آبکاری با روش های گوناگون زیر انجام می شود:
۱-آبکاری با جریان الکتریسیته:مانند آبکاری طلا-مس-نقره- تیتانیوم-کرم و نیکل….
۲-آبکاری الکترولس (electroless) بدون نیاز به جریان الکتریسیته:مانند ابکاری الکترولس مس و نیکل با دما و زمان
۳-آبکاری به روش حرارتی:مانند گالوانیزه گرم با روی و ملغمه کاری با طلا و سفید کاری با قلع
با این روش ها می توان یک پوشش فلزی با ضخامت ۵ تا ۳۰ میکرون و گاهی بیشتر از آن را روی فلزات متصل نمود .این عملیات علاوه بر ایجاد زیبایی، از قطعه در برابر خوردگی محافظت می کند.از ویژگی های دیگر آبکاری ایجاد یک پوشش مانند طلا و نقره برای انتقال بهتر جریان الکتریسیته می باشد. برخی آبکاری ها مقاومت سایشی را نیز افزایش می دهند. امروزه برای پوشش کاری روش های جدیدی مانند PVD CVD و کلدینگ ،متال اسپری …. ابداع و مورد استفاده قرار گرفته است.
برگرفته از دپارتمان شیمی


برای نوشتن دیدگاه وارد حساب کاربری خود شوید.