واکنشهای ساعتی یکی از منحصر به فرد ترین دستههای واکنشهای شیمیایی است که واکنشهای ساعتی Landolt از معروف ترین آنهاست.
در نوع واکنش خاص، دو محلول بیرنگ با یکدیگر مخلوط میکنیم. در لحظات ابتدایی اتفاق خاصی مشاهده نمیشود ولی بعد از چند دقیقه ناگهان رنگ محلول از بیرنگ به آبی تیره تغییر میکند. به عبارت دیگر میتوان مکانیزم وکنشهای ساعتی را چنین بیان کرد که با مخلوط محلولها (بیرنگ) فوراً تغییری که با چشم بتوان آن را دید، مشاهده نمیشود اما رنگ محلول بعد از گذشت زمانی به طور ناگهانی تغییر میکند، که از این زمان به زمان انجام واکنش تعبیر میشود.
چگونگی انجام واکنشهای ساعتی
در این سیستم A,B,C,D واکنش دهنده میباشند. در این سیستم ابتدا واکنش گر A با واکنش گر B واکنش میدهد و محصول P را میدهد.
A + B → P
واکنش شماره یک
اکنون P تشکیل شده با واکنش گر C واکنش میدهد و مصرف میشود و محصول R را میدهد.
P + C → R
واکنش شماره دو
اگر غلظت A و B به اندازه کافی بالا باشد (نسبت به غلظت C) مصرف واکنش گر C تاثیر کلی را بر واکنشهای ۱ و ۲ خواهد گذاشت. به مجرد آنکه واکنش گر C به طور کلی از سیستم واکنش حذف شود محصول تولیدی واکنش 1 (P) دیگر واکنش نمیدهد به همین دلیل غلظت مادهٔ P به سرعت بالا میرود. دراین حالت (نقطه بحرانی) که غلظت ماده P به اندازه کافی برای واکنش با واکنش گر چهارم (D) بالا رود، واکنش زیر که منجر به تولید محصول رنگی و خود باعث تغییر رنگ محلول میشود، انجام میپذیرد.
P + D → Colored product
واکنش شماره سه
این نکته نیز شایان ذکر است که سرعت واکنش ۲ باید بیشتر از سرعت واکنش ۳ باشد. (که P با C واکنش دهد نه D.)
شناخته شده ترین واکنشهای ساعتی، واکنشهای Landolt است.
که در آن واکنش بین یونهای ید و پرسولفات مورد بررسی قرار میگیرد.
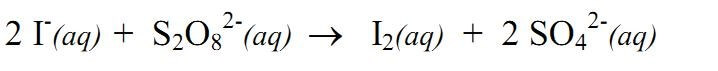
سرعت واکنش با افزایش مقدار ناچیزی یون تیوسولفات اندازهگیری میشود و ید آزاد شده از واکنش بالا سریعاً با تیوسولفات واکنش داده و به I- تبدیل میشود.
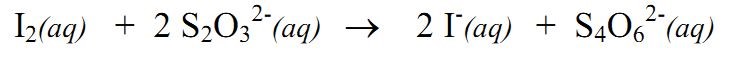
این عمل ادامه مییابد تا وقتی که همه تیوسولفات به تتراتیونات تبدیل شود. در این صورت ید تولید شده از واکنش اول به صورت آزاد باقی میماند. از معرف چسب نشاسته برای نشان دادن این حالت استفاده میشود. بدین ترتیب که یون آزاد شده با چسب نشاسته تولید رنگ آبی میکند.
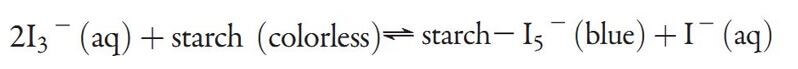
فاصله زمانی از شروع واکنش تا ظاهر شدن رنگ آبی معیاری از سرعت اولیه واکنش است. واکنشهایی نظیر این واکنش را تحت عنوان واکنشهای سرعتی معرفی میکنند و این واکنش را نیز ساعت یدی میگویند.
آزمایش واکنش ساعتی ید نمونهای از واکنش ساعتی
سرعت این واکنش مانند اکثر واکنش ها به غلظت و دما بستگی دارد، با تغییر و ازدیاد غلظت هریک از واکنشگرها سرعت افزایش می یابد.
آزمایش کلی به این ترتیب است که ابتدا با افزایش آب اکسیژنه به مخلوط سولفوریک اسید و (پتاسیم یدید)KI می توان ید تهیه نمود.
2KI + H2SO4 + H2O2 → K2SO4 + I2 + 2H2O
ید رنگ نشاسته موجود در مخلوط آزمایش را آبی می کند، حال اگر به این مخلوط تیوسولفات اضافه شود، ید وارد واکنش می شود و رنگ آبی کم کم ازبین می رود.
I2 + 2 Na2S2O3 → 2NaI + Na2S4O6
چنانچه ید اضافی باقی بماند سبب آبی رنگ شدن نشاسته می شود.
نحوه آزمایش به این شکل است که ابتدا محلولی از مخلوط پتاسیم یدید و سدیم تیوسولفات با غلظت مشخص و معین تهیه می کنند (محلول الف) سپس درچند لوله آزمایش به تساوی حجم ثابتی از این محلول ریخته و به آن ها حجم مناسبی سولفوریک اسید رقیق و چند قطره چسب نشاسته می افزایند (لوله های A).
به همان تعداد درچند لوله آزمایش دیگر محلول پر اکسید هیدروژن که با غلظت معین رقیق نموده اند. با حجم های مثلا 5 ، 10 ، 15 ، ... آماده می کنند. (لوله های B)
در مرحله آخر همزمان هر یک از محلول های لوله های (A) را به محتویات لوله های (B) می افزایند و زمان انجام واکنش را در هر لوله آزمایش اندازه گیری می کنند. چون حجم محلول در لوله های B به یک اندازه افزایش یافته فاصله زمان انجام واکنش درآن ها برابر خواهد بود.
منبع:ویکیپدیا - راسخون




برای نوشتن دیدگاه وارد حساب کاربری خود شوید.